 Numeroase studii au arătat, totuși, că indivizii care au anumite variații genetice frecvente, pot avea un risc crescut de boli, în condițiile în care dieta acestora, deși conformă cu recomandările generale, nu este adecvată particularităților genetice specifice acestor indivizi. Pentru a aborda această problemă, oamenii de știință au apelat la studierea relației dintre gene și mediu (gene-environment interactions) și, respectiv a relației dintre gene și nutriție (gene-nutrient interactions). Astfel, nutriția este socotită ca un factor de mediu.
Numeroase studii au arătat, totuși, că indivizii care au anumite variații genetice frecvente, pot avea un risc crescut de boli, în condițiile în care dieta acestora, deși conformă cu recomandările generale, nu este adecvată particularităților genetice specifice acestor indivizi. Pentru a aborda această problemă, oamenii de știință au apelat la studierea relației dintre gene și mediu (gene-environment interactions) și, respectiv a relației dintre gene și nutriție (gene-nutrient interactions). Astfel, nutriția este socotită ca un factor de mediu.
Rezultatele acestor studii au arătat că, pentru anumite gene ale căror funcții sunt strâns legate de metabolismul nutrienților, anumite variații genetice pot fi, în funcție de nutriție, fie benefice, fie dăunătoare, și că noțiunea de gene ,,bune” sau ,,rele” nu are sens. Mai degrabă, rolul benefic sau dăunător al unor variații genetice trebuie judecat în contextul aportului nutritiv și în contextul unei populații sau rase umane specifice, care trăiește într-un anumit context ecologic (inclusiv nutrițional).
Pentru a înțelege rolul mediului în contextualizarea rolului genelor asupra stării de sănătate, discutăm mai jos exemplul genelor FADS1/FADS2 în definirea necesarului de acizi grași omega-3 și omega-6.
–
Rolul haplotipurilor FADS1/2 in definirea necesarului de acizi grași polinesaturați omega-3 și omega-6 (PUFA)
Acizii grași omega-3 și omega-6 sunt două categorii distincte de nutrienți, cu roluri fiziologice distincte. Dacă acizii omega-6 sunt esențiali pentru dezvoltarea și creșterea țesuturilor, acizii omega-3 sunt implicați atât în modularea proceselor inflamatorii, cât și în modularea proceselor de coagulare a sângelui. Alte numeroase roluri au fost identificate, inclusiv în definirea structurii membranelor celulare, maturizarea celulelor precursoare de neuroni, transportul colesterolului și exportul acestuia din ficat, etc.
Important este să reținem ca acești nutrienți sunt necesari pentru funcționarea normală a organismului uman. De asemenea, este important să știm că, deși sunt două categorii diferite de nutrienți, acizii omega-3 și omega-6 sunt metabolizați sub controlul acelorași gene. Dintre acestea, genele FADS1 și FADS2 controlează rata la care acești acizi grași sunt transformați prin desaturare, un proces chimic care adaugă legături covalente duble în interiorul acestor molecule. Așa se face că precursorii PUFA (care sunt acidul linoleic pentru clasa omega-6, și acidul alfa-linolenic pentru clasa omega-3) sunt transformați, sub controlul acelorași gene, în alți compuși activi precum acidul arahidonic (ARA, omega-6) sau acizii eicosapentaenoic (EPA) și docosahexaenoic (DHA) pentru clasa omega-3. Cam complicat, nu-i așa? Nu trebuie să rețineți aceste lucruri, ci doar faptul că genele FADS1 și FADS2 controlează rata de metabolizare (în paralel) a acestor acizi grași.
În natură, omul are acces la două mari surse de acizi PUFA: cele de origine vegetală care conțin precursorii de care vorbeam mai sus, adică acidul linoleic pentru omega-6 și acidul alfa-linolenic pentru omega-3, și alimente de origine marină (pește, scoici, etc) care conțin produșii de metabolism ARA, EPA și DHA, aceasta deoarece doar organismele superioare (peștele inclusiv) sunt capabile de această conversie.
Pe de altă parte, genele FADS1 și FADS2 conțin multiple variații genetice acumulate de-a lungul evoluției umane. Așa se face că în prezent, aceste gene au acumulat sute de variații genetice, în diferite regiuni ale acestor gene. Interesant însă, cercetătorii au constatat, folosind secvențiererea genomurilor a mii de indivizi, că aceste variații genetice sunt prezente doar în anumite combinații. In final, au realizat că, pentru 95% din populație, aceste variații genetice se găsesc în doar două combinații (numite haplotipuri): haplotipul A este prezent în 40% din indivizi, iar haplotipul D în 55% din indivizi. Restul de 5% din populația globului au combinații foarte rare, sau nu se pot clasifica într-o combinație anume de variații genetice.
Analizând genomul speciilor anterioare celei de Homo sapiens, specialiștii au constatat că acestea posedau doar 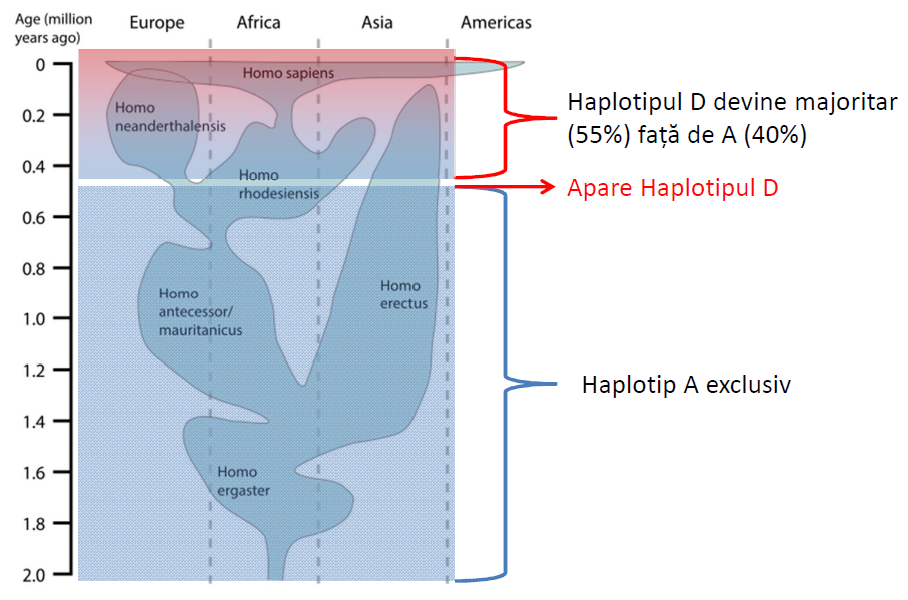 haplotipul A, care metaboliza acizii PUFA mai lent. Undeva inainte de apariția lui Homo sapiens (vezi figura alăturată), au apărut o serie de mutații genetice, care mai apoi s-au grupat în Haplotipul D, prezent azi în 55% din populația lumii. Aceste haplotip este caracterizat de o capacitate crescută de metabolizare a acizilor PUFA, și deci de sinteză a acizilor ARA, EPA si DHA, adică acele molecule care sunt benefice creșterii organismului și dezvoltării creierului. În condițiile în care oamenii din vechime aveau un aport nutritiv de omega-6 și omega-3 intr-o proporție de 1/1, apariția haplotipului D a adus un avantaj evolutiv posesorilor acestui haplotip, fapt demonstrat și de creșterea frecvenței populației cu acest haplotip, de la 0% la 55%.
haplotipul A, care metaboliza acizii PUFA mai lent. Undeva inainte de apariția lui Homo sapiens (vezi figura alăturată), au apărut o serie de mutații genetice, care mai apoi s-au grupat în Haplotipul D, prezent azi în 55% din populația lumii. Aceste haplotip este caracterizat de o capacitate crescută de metabolizare a acizilor PUFA, și deci de sinteză a acizilor ARA, EPA si DHA, adică acele molecule care sunt benefice creșterii organismului și dezvoltării creierului. În condițiile în care oamenii din vechime aveau un aport nutritiv de omega-6 și omega-3 intr-o proporție de 1/1, apariția haplotipului D a adus un avantaj evolutiv posesorilor acestui haplotip, fapt demonstrat și de creșterea frecvenței populației cu acest haplotip, de la 0% la 55%.
Cu alte cuvinte, nu a fost rău că unii indivizi au avut haplotipul D.
Problema însă apare în contextul nutriției din zilele noastre, în care avem un aport exagerat de omega-6 față de omega-3. Intrucât haplotipul D accelerează metabolismul acizilor omega-6, posesorii haplotipului D produc azi prea mulți acizi omega-6. Și, din păcate, excesul de omega-6 duce la apariția bolilor cardiovasculare, inclusiv a bolilor coronariene. Astăzi, posesorii haplotipului D au un risc crescut de a muri din cauze cardiovasculare. Pe de altă parte, posesorii haplotipului A (cel inițial) au riscul mai mic de a se imbolnăvi de boli cardiovasculare, independent de aportul de omega-6 (acid linoleic) pe care îl au.
Cu alte cuvinte, dacă haplotipul D a fost în trecut, avantajos pentru oameni, astăzi acesta este dezavantajos, dar aceasta DOAR în contextul în care nutriția noastră s-a modificat înspre un aport mai mare de omega-6 față de aportul de omega-3.
Acest exemplu a fost discutat pentru a înțelege relația dintre structura genetică a fiecărui individ, și legătura acesteia cu aportul nutritiv. Evident, soluții există, și anume a afla tocmai care sunt variațiile genetice ale fiecăruia și cum, în funcție de acestea, un individ își poate modifica dieta (cu ajutorul unui specialist) potrivit necesarului optim definit de propriul genom. Această nouă abordare se numește nutriție de precizie și este motivul pentru care Advanced Nutigenomics oferă testul nutrigenetic Advanced NGx.
